Benzoylchlorid
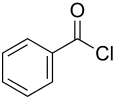
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Benzoylchlorid | ||||||||||||||||||
| Andere Namen |
|
||||||||||||||||||
| Summenformel | C7H5ClO | ||||||||||||||||||
| Kurzbeschreibung |
farblose, an feuchter Luft rauchende, tränenreizende Flüssigkeit mit stechendem Geruch |
||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 140,57 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig |
||||||||||||||||||
| Dichte |
1,22 g·cm−3 |
||||||||||||||||||
| Schmelzpunkt |
−1 °C |
||||||||||||||||||
| Siedepunkt |
197 °C |
||||||||||||||||||
| Dampfdruck |
50 Pa (20 °C) |
||||||||||||||||||
| Löslichkeit |
Zersetzung in Wasser |
||||||||||||||||||
| Brechungsindex |
1,5537 (20 °C) |
||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| MAK |
nicht festgelegt, da Verdacht auf krebserzeugende Wirkung |
||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||
Benzoylchlorid ist eine chemische Verbindung aus der Stoffgruppe der Carbonsäurechloride. Es handelt sich um das Säurechlorid der Benzoesäure.
Inhaltsverzeichnis
Gewinnung und Darstellung
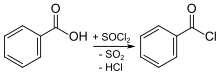
Benzoylchlorid lässt sich durch die Umsetzung von Benzoesäure mit Thionylchlorid oder Phosphortrichlorid synthetisieren.
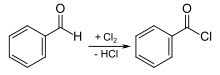
Wichtigste Methoden der industriellen Herstellung des Benzoylchlorids sind jedoch die Chlorierung von Benzaldehyd:
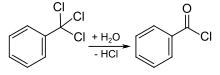
sowie die kontrollierte Hydrolyse von Benzotrichlorid:
oder dessen Reaktion mit Benzoesäure:
Eigenschaften
Benzoylchlorid ist eine schwer entzündliche, farblose Flüssigkeit (Flammpunkt zwischen 55 und 100 °C), deren Dämpfe mit Luft beim Erhitzen des Stoffes über seinen Flammpunkt ein explosionsfähiges Gemisch bilden können. An feuchter Luft ist die Chemikalie infolge der Zersetzung zu Chlorwasserstoff und Benzoesäure leicht rauchend.
Reaktionen
Benzoylchlorid reagiert mit Wasser in einer Hydrolysereaktion zu Benzoesäure und Salzsäure. Durch Reaktion mit Ammoniak lässt sich Benzamid herstellen und durch die Umsetzung mit Alkoholen sind die entsprechenden Benzoesäureester zugänglich.
Verwendung
Benzoylchlorid wird u. a. zur Herstellung von Benzoesäureestern verwendet. Wegen seiner Schwerlöslichkeit in Wasser kann die Veresterung gut nach der Schotten-Baumann-Methode durchgeführt werden. Die Verwendung von Carbonsäurechloriden anstelle der Carbonsäuren liefert deutlich höhere Ausbeuten.
In der Nucleinsäurenchemie dient Benzoylchlorid in Pyridin als Lösungsmittel als beliebtes Reagens zur Einführung der Benzoyl-Schutzgruppe, um sekundäre Alkohole zu schützen. Die Schutzgruppe kann durch alkalische Hydrolyse des Benzoesäureesters leicht wieder entfernt werden.
Sicherheitshinweise
Beim Kontakt mit Wasser (z. B. aus der Luft) entstehen gefährliche Chlorwasserstoff-Dämpfe. Benzoylchlorid verursacht auf der Haut schmerzhafte Verätzungen. Die unangenehm und stechend riechenden Dämpfe reizen Atemwege und Augen. Im Tierversuch erwies sich Benzoylchlorid (wahrscheinlich wegen der extrem schnellen Metabolisierung zu Benzoesäure, Hippursäure und Chlorwasserstoff) nicht als genotoxisch. Aussagen zur Kanzerogenität können zurzeit nicht getroffen werden.