
Glial Cell Line-derived neurotrophic Factor
| Glial Cell Line-derived neurotrophic Factor | ||
|---|---|---|
| ||
| Eigenschaften des menschlichen Proteins | ||
| Bezeichner | ||
| Gen-Name | GDNF | |
| Externe IDs | ||
Glial cell line-derived neurotrophic factor (GDNF) ist ein Protein, welches beim Menschen durch das GDNF-Gen kodiert wird und das Überleben vieler Arten von Neuronen fördert. Es wird durch GFRα-Rezeptoren, insbesondere GFRα1, signalisiert. Es ist auch für die Bestimmung von Spermatogonien zu primären Spermatozyten verantwortlich, d. h., es wird vom RET-Proto-Onkogen (RET) empfangen und teilt durch Bildung eines Gradienten mit SCF die Spermatogonien in zwei Zellen. Infolgedessen kommt es zur Retention von Spermatogonien und zur Bildung von Spermatozyten.
Inhaltsverzeichnis
Die GDNF-Ligandenfamilie (GFL)
GDNF wurde 1991 als erstes Mitglied der GDNF-Ligandenfamilie entdeckt.
Funktion
GDNF ist sowohl im peripheren als auch im zentralen Nervensystem weit verbreitet. Es kann von Astrozyten, Oligodendrozyten, Schwann-Zellen, Motoneuronen und Skelettmuskeln während der Entwicklung und des Wachstums von Neuronen und anderen peripheren Zellen sezerniert werden.
Das GDNF-Gen kodiert einen hoch konservierten neurotrophen Faktor. Es wurde gezeigt, dass die rekombinante Form dieses Proteins das Überleben und die Differenzierung dopaminerger Neuronen in Kultur fördert und die durch Axotomie ausgelöste Apoptose von Motoneuronen verhindern kann. GDNF wird als 211 Aminosäuren langer Proteinvorläufer, pro-GDNF, synthetisiert. Die Prä-Sequenz führt das Protein zur Sekretion in das endoplasmatische Retikulum. Während der Sekretion faltet sich der Proteinvorläufer über eine Sulfid-Sulfid-Bindung und dimerisiert. Während der Verpackung und Aufbereitung im Golgi-Apparat wird das Protein dann durch N-gebundene Glykosylierung modifiziert. Schließlich wird der Proteinvorläufer aufgrund einer proteolytischen Konsensussequenz an seinem C-Terminus einer Proteolyse unterzogen und damit in seine reife Form mit 134 Aminosäuren überführt. Zu den Proteasen, die bei der Proteolyse von pro-GDNF zu reifem GDNF eine Rolle spielen, gehören Furin, PACE4, PC5A, PC5B und PC7. Da mehrere Proteasen den Proteinvorläufer spalten können, können vier verschiedene reife Formen von GDNF produziert werden. Die proteolytische Verarbeitung von GDNF erfordert SorLA, einen Rezeptor für die Proteinsortierung. SorLA bindet an keine anderen GFLs. Die reife Form des Proteins ist ein Ligand für das Produkt des Protoonkogens RET (rearranged during transfection). Neben dem Transkript, das für GDNF kodiert, wurden auch zwei weitere alternative Transkripte beschrieben, die für unterschiedliche Proteine kodieren, die als astrozytäre trophische Faktoren bezeichnet werden. Mutationen in diesem Gen können mit der Hirschsprung-Krankheit in Verbindung gebracht werden.
GDNF ist in der Lage, die ERK-1- und ERK-2-Isoformen der MAP-Kinase in sympathischen Neuronen sowie den PI3K/AKT-Signalweg über die Aktivierung seiner Rezeptortyrosinkinasen zu aktivieren. Über seinen GFRα1-Rezeptor kann er auch Kinasen der Src-Familie aktivieren.
Die auffälligste Eigenschaft von GDNF ist seine Fähigkeit, das Überleben von dopaminergen und motorischen Neuronen. Es verhindert die Apoptose in motorischen Neuronen während der Entwicklung, verringert den Gesamtverlust von Neuronen während der Entwicklung, rettet Zellen vor dem axotomie-induzierten Tod und verhindert die chronische Degeneration.
Diese Neuronenpopulationen sterben im Verlauf der Parkinsonschen Krankheit und der amyotrophen Lateralsklerose (ALS) ab. GDNF reguliert auch die Nierenentwicklung und die Spermatogenese und hat in Ratttenversuchen eine starke und schnelle negative (verbessernde) Wirkung auf den Alkoholkonsum. GDNF fördert auch die Bildung von Haarfollikeln und die Wundheilung der Haut, indem es auf die im Bulge-Kompartiment ansässigen Haarfollikel-Stammzellen (BSCs) abzielt.
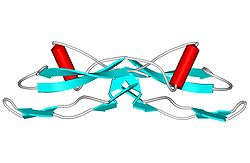
Struktur
Die Struktur von GDNF ähnelt der von TGFβ2. GDNF besitzt zwei fingerartige Strukturen, die mit dem GFRα1-Rezeptor interagieren. Die N-gebundene Glykosylierung, die während der Sekretion von pro-GDNF erfolgt, findet an der Spitze einer der fingerartigen Strukturen statt. Der C-Terminus des reifen GDNF spielt eine wichtige Rolle bei der Bindung sowohl an Ret als auch an den GFRα1-Rezeptor. Der C-Terminus bildet eine Schleife aus den Wechselwirkungen zwischen den Cysteinen Cys131, Cy133, Cys68 und Cys 72.
Interaktionen
Es wurde gezeigt, dass der Glial cell line-derived neurotrophic factor mit GFRA1 und dem Rezeptor alpha 1 der GDNF-Familie interagiert. Die Aktivität von GDNF und anderen GFLs wird durch die Rezeptortyrosinkinase RET vermittelt. Damit der Rezeptor die GDNF-Aktivität modulieren kann, muss GDNF auch an GFRα1 gebunden sein. Die Intensität und Dauer der RET-Signalisierung kann ebenfalls durch den GPI-Anker von GFRα1 überwacht werden, indem er mit Kompartimenten der Zellmembran interagiert, z. B. Lipid Rafts oder Spaltung durch Phospholipasen. In Zellen, denen RET fehlt, können einige Liganden der GDNF-Familie auch durch das neurale Zelladhäsionsmolekül (NCAM) aktiviert werden. GDNF kann über seinen GFRα1-GPI-Anker mit NCAM assoziieren. Die Assoziation zwischen GDNF und NCAM führt zur Aktivierung der zytoplasmatischen Protein-Tyrosin-Kinasen Fyn und FAK.
Therapeutisches Potential
GDNF wurde als Mittel zur Behandlung der Parkinson-Krankheit erforscht, obwohl frühe Forschungsarbeiten keine signifikante Wirkung zeigten.
Im Jahr 2012 begann die Universität Bristol eine fünfjährige klinische Studie mit Parkinson-Patienten, bei der Chirurgen jedem der 41 Teilnehmer einen Port in den Schädel einführten, durch den das Medikament direkt zu den geschädigten Zellen gelangen konnte. Die Ergebnisse der Doppelblindstudie, bei der die Hälfte der Teilnehmer nach dem Zufallsprinzip regelmäßige GDNF-Infusionen und die andere Hälfte Placebo-Infusionen erhielt, zeigten keinen statistisch signifikanten Unterschied zwischen der aktiven Behandlungsgruppe und denjenigen, die ein Placebo erhielten, bestätigten aber die Auswirkungen auf die geschädigten Gehirnzellen. Die Studie wurde von Parkinson's UK mit Unterstützung des Cure Parkinson's Trust finanziert, dessen Gründer Tom Isaacs einer der Teilnehmer war.
Neuropsychopharmakologie
Es gibt Hinweise darauf, dass Gdnf ein auf Alkohol reagierendes Gen ist, das bei kurzfristigem Alkoholkonsum hochreguliert wird, während es beim Entzug von übermäßigem Alkoholkonsum herunterreguliert wird. Eine Studie konnte zeigen, dass Alkoholentzug die Expression von Gdnf in mit Sucht zusammenhängenden Hirnbereichen wie dem ventralen tegmentalen Areal (VTA) und dem Nucleus Accumbens sowie die DNA-Methylierung des Gdnf-Gens bei Ratten verändert.