
Multiples Myelom
| Klassifikation nach ICD-10 | |
|---|---|
| C90.0 | Multiples Myelom |
| C90.3 | Solitäres Plasmozytom |
| ICD-10 online (WHO-Version 2019) | |
| Klassifikation nach ICD-O-3 | |
|---|---|
| 9732/3 | Multiples Myelom (C42.1) |
| 9731/3 | Plasmozytom o.n.A., Solitäres Myelom |
| ICD-O-3 erste Revision online | |
Das Multiple Myelom (MM), kurz auch Myelom, häufig synonym verwendet Plasmozytom (früher auch myelogenes Plasmocytom) und weniger gebräuchlich: Plasmazellmyelom, Kahler-Krankheit bzw. Kahlersche Krankheit nach Otto Kahler und Huppert-Krankheit nach Karl Hugo Huppert, ist eine von den Plasmazellen des Knochenmarks ausgehende Krebserkrankung, ein Non-Hodgkin-Lymphom des blutbildenden Systems. Das Multiple Myelom wird übergeordnet zu den Monoklonalen Gammopathien gezählt. Es ist gekennzeichnet durch eine krankhafte (unkontrollierte) Vermehrung Antikörper-produzierender Zellen, der Plasmazellen (ausdifferenzierte B-Zellen). Die entarteten Plasmazellen produzieren in der Regel Antikörper oder Teile/Bruchstücke davon (z. B. freie Leichtketten). Da ein maligner Plasmazellklon von einer gemeinsamen Vorläuferzelle abstammt, sind sie genetisch weitgehend identisch und produzieren ebenso identische (= monoklonale) Antikörper. Nah verwandt, aber abzugrenzen vom Multiplen Myelom sind die Plasmazell-Leukämie, das extramedulläre Plasmozytom und das solitäre Plasmozytom.
Dem Multiplen Myelom geht immer eine Monoklonale Gammopathie unklarer Signifikanz (MGUS) voraus. Eine MGUS muss nicht zwangsläufig zu einer malignen Erkrankung führen. Häufig gehen aber verschiedene Komorbiditäten/Komplikationen auch ohne die Entwicklung einer hämatologischen Erkrankung damit einher. Als Übergangsstufe zwischen MGUS und MM gilt das schwelende Multiple Myelom (smouldering myeloma; SMM). Der Grad der Malignität eines MM kann sehr unterschiedlich sein und reicht von einem nur langsam fortschreitenden MM bis hin zu einer aggressiven, schnell fortschreitenden Verlaufsform, die häufig durch entdifferenzierte, plasmoblastische Plasmazellen gekennzeichnet ist.
Inhaltsverzeichnis
Zur Terminologie und Medizingeschichte
Einordnung ins System hämato-onkologischer Erkrankungen
Das Multiple Myelom zählt zu den indolenten (niedrig-malignen) B-Zell-Non-Hodgkin-Lymphomen. Vom echten Multiplen Myelom ist der Begriff Plasmozytom abzugrenzen, der nur ein isoliertes Myelom bezeichnet, bei dem die Erkrankung auf einen einzigen lokalen Krankheitsherd (in der Regel eine Osteolyse = lokale Knochenauflösung) begrenzt ist:
„Im angloamerikanischen Sprachraum wird die als ‘multiple myeloma’ bezeichnete Erkrankung streng von dem ‘plasmocytoma’ getrennt. Diese Trennung sollte auch in der deutschen Terminologie erfolgen, denn ein ‘Plasmozytom’ ist laut Definition ein ‘solitärer Tumor aus Plasmazellen’ ... Finden sich mehrere Plasmazelltumoren, so beschreibt der Terminus ‘Multiples Myelom’ diese Form der Plasmazellenerkrankung am besten.“
So unterscheidet denn auch die ICD-10 Klassifikation der WHO strikt zwischen C90.0 Multiples Myelom und C90.03 Solitäres Plasmozytom.
In Deutschland ist allerdings im allgemeinen klinischen Sprachgebrauch eine weitgehend synonyme Verwendung der beiden Begriffe verbreitet, weshalb mit Plasmozytom häufig ein Multiples Myelom gemeint ist.
Abzugrenzen vom Multiplen Myelom/Plasmozytom sind die Vorstufen Schwelendes Multiples Myelom (SMM) sowie die Monoklonale Gammopathie unklarer Signifikanz (MGUS), bei denen ebenfalls eine klonale Immunglobulinproduktion vorliegt. Symptome und Komplikationen können aber auch schon bei den Vorstufen auftreten, was jedoch aufgrund fehlender Kriterien nicht zwangsläufig zur Diagnose Multiples Myelom führt. Um eine differenziertere Beurteilung der Patienten zu ermöglichen, wurde für Patienten mit nephrologischen Komplikationen, welche auf eine klonale Immunglobulinproduktion krankhaft veränderter Plasmazellen zurückzuführen sind, der Terminus Monoklonale Gammopathie renaler Signifikanz (MGRS) eingeführt. Weitere Monoklonale Gammopathien, die nicht als Multiples Myelom bezeichnet werden, sind die AL-Amyloidose (diese kann aber auch zusätzlich zu einem Multiplen Myelom auftreten) und der Morbus Waldenström. Seit einiger Zeit wird aufgrund der Komplexität der Erkrankung(en) und der teilweise schwer abzugrenzenden Vorstufen sowie nahverwandten Entitäten eine Reform der Terminologie diskutiert. Hierbei soll zwischen einer Monoklonalen Gammopathie, bei der eine Behandlung notwendig ist, und einer solchen, die ohne Komplikationen nur unter Beobachtung steht, unterschieden werden.
Etymologie
Der medizinische Fachbegriff ‘Myel-om’, übersetzt ‘Knochenmark-Geschwulst’, ist ein Neologismus, eine Wortbildung, geschaffen durch Derivation aus dem Substantiv altgriechisch μυελός „myelós“, ‘Knochen-Mark’ und dem Suffix ‘-om’, von altgriechisch ωμ(α) „ōm(a)“.
Dabei ist allerdings das dem Griechischen entlehnte Suffix „-om“ kein Lexem, sondern ein Wortbildungs-Morphem ohne begriffliche Bedeutung. Ein Lexem, also ein Nomen, ein Substantiv „ωμ(α)“, „ōm(a)“ hat es im Altgriechischen niemals gegeben.
In der modernen medizinischen Terminologie dagegen nimmt dieses Suffix „-om“ den Rang eines Lexems, eines Appellativums ein, dem international die Bedeutung Geschwulst zugewiesen worden ist.
„Zu der Zeit nun, da die moderne Medizin als Korrelat für die immer mehr nach Lage, histologischer Struktur usw. spezifizierten Geschwulste ein differenzierteres terminologisches Reservoir benötigte und in bewährter Weise griechisches und/oder lateinisches Material fur Neologismen adaptierte, lag es nahe, den gemeinsamen Nenner in der Sache (= Geschwulst) auch formal als konstantes Element der Wortbildung sichtbar zu machen. So wählte man die Gruppe der Bildungen auf „ωμ(α)“, „ōm(a)“ des Altgriechischen („καρκίν-ωμα“, Karkinōma, „σάρκωμα“, Sarkoma u. a. m.) als Muster und bildete danach die rein griechischen Termini Karzinom, Sarkom u. a. m.“
So wurde das Wortbildungs-Morphem „-om“ von den medizinischen Terminologen sekundär mit lexikalischer Bedeutung aufgefüllt und das Stadium erreicht, in dem ein ursprüngliches Morphem den Rang eines Lexems, eines Appellativums, einnimmt.
Die wörtliche Übersetzung des medizinterminologischen Kunstwortes „Myel-om“, Englisch “myeloma”, ins Deutsche lautet also „Knochenmark-Geschwulst“, Knochenmarkkrebs.
Wortgeschichte
“The term ‘multiple myeloma’ was introduced by von Rustitzky in 1873 when he found eight separate tumors of bone marrow and designated them ‘multiple myelomas’. In Russia, the term Rustitzky’s disease is often used.”
„Der Terminus ‘Multiples Myelom’ wurde von Rustitzky im Jahre 1873 eingeführt, als er acht getrennt liegende Knochenmarktumore vorfand. Er bezeichnete sie als ‘Multiple Myelome’. In Russland ist die Bezeichnung Rustitzkys Krankheit weit verbreitet.“
Um das Gebundensein von Tumoren an das Knochenmark zu charakterisieren, führte der Chirurg J. von Rustitzky im Jahre 1873, nach Autopsie des 47 Jahre alten Knechtes Joh. Kessler, die Bezeichnung Myelom in die medizinische Terminologie ein.
„Die mikroskopische wie makroskopische Beschaffenheit obiger Tumoren berechtigt uns, sie als eine besondere Klasse einzustellen und ihnen, um die Identität ihrer Struktur mit dem Knochenmark zu bezeichnen, den Namen ‚Myelome‘ zu geben.“
Rustitzky interpretierte damals, um das Jahr 1873, diese Erkrankung, „deren ursächliches Moment uns unbekannt bleibt“, als eine gutartige, lokale Hypertrophierung des Knochenmarks:
„Dieses Gebundensein der Tumoren an das Knochenmark berechtigt ferner zur Behauptung, dass die vorliegenden Tumoren, obwohl multipel, nicht im strengen Sinne bösartig waren … Vielmehr scheint es geratener, diese Tumoren den sonstigen gutartigen, aber multipel auftretenden Tumoren (Adenome, Lipome, Fibrome, Exostosen etc.) anzureihen und eine lokale Erkrankung des Knochenmarks, als Auslegung der Tumorbildung, zu betrachten, und diese Erkrankung, deren ursächliches Moment uns nicht bekannt ist, als Hypertrophierung des Knochenmarkgewebes zu bezeichnen.“
In den Folgejahren zeigen Titel von Fachaufsätzen, wie der von Rustitzky vorgeschlagene Ausdruck Multiples Myelom zum akzeptierten terminologischen Allgemeingut wurde, und wie die langsam fortschreitende medizinische Forschung nach und nach mehr Licht in das Dunkel „des uns unbekannten ursächlichen Momentes dieser Erkrankung“ brachte.
Hippokrates hat diesen langsamen wissenschaftsgeschichtlichen Prozess im 5. Jahrhundert v. Chr. durch einen Aphorismus auf den Punkt gebracht: Ars longa, vita brevis, frei übersetzt: die Heilkunst schreitet langsam voran, und das Leben ist kurz.
Medizingeschichte

Das Multiple Myelom ist keine Erscheinung der Neuzeit, bereits seit vielen Jahrhunderten werden Menschen von dieser Erkrankung heimgesucht:
„Die Arbeitsgruppe von A. Zink aus dem Pathologischen Institut der LMU München untersuchte im Rahmen der Paläopathologie 415 ägyptische Mumien (1500–500 v. Chr.). Bei vier von diesen zeigten sich maligne Skelettveränderungen, bei zwei Mumien multiple, myelomverdächtige Osteolysen an Wirbelsäule, Becken und Schädel.“
Auch Knochenfunde aus dem 2. Jahrhundert v. Chr. weisen die typischen zerstörerischen Merkmale der Erkrankung auf.
Historischer Fallbericht: Thomas McBean (1850):
Der erste gut dokumentierte Fall eines Multiplen Myeloms geht auf einen Fallbericht von Macintyre zurück. Er beschrieb die Krankheitsgeschichte des englischen Gemischtwarenhändlers Thomas A. McBean, welcher sich 1845 im Alter von 45 Jahren in seiner Arztpraxis vorgestellt hatte. McBean beklagte, dass etwas mit seinem Urin nicht stimmte – er verspürte häufig Harndrang, und sein „Leibkleid wurde durch den Urin ganz steif“, obwohl er keinen Ausfluss aus der Harnröhre bemerkt hatte. Außerdem litt der Patient an ungewöhnlicher Schwäche und Ausgezehrtheit, während eines Spaziergangs habe er dann das Gefühl gehabt, „etwas im Brustkorb knackte oder gab nach“, und McBean stürzte und konnte sich „wegen starker Schmerzen für einige Minuten nicht mehr erheben“. Doktor Macintyre behandelte den Patienten mit einer Bandage des Brustkorbes („strengthening plasters“) und verordnete körperliche Schonung. Einen Monat später hatte der Patient erneut starke Schmerzen, woraufhin man wiederholte Aderlässe, Blutegelbehandlungen und Schröpfkegel einsetzte, was jedoch keine dauerhafte Linderung brachte, so dass sich McBean bei einem anderen Arzt, Dr. Watson, vorstellte. Dieser begann eine Behandlung mit Eisen und Chinin, was zu einer erstaunlichen Besserung führte, die ein halbes Jahr anhielt. Im Oktober 1845 erlitt der Patient jedoch starke Schmerzen an der Wirbelsäule und dem Ischias, welche sich auch durch den Einsatz von warmen Bädern, Campherpuder und -salbe nicht besserten. Dr. Macintyre diagnostizierte außerdem Ödeme am Körper von McBean und untersuchte daher den Urin des Patienten. Dieser war dunkel und flockte bei Erhitzung aus („abound in animal matter“). Fast gleichzeitig schickte Watson mit der Frage „What is it?“ eine Urinprobe an den Arzt und Chemiker Bence Jones, welcher Proteine im Urin von McBean – und anderer Patienten mit ähnlichen Beschwerden – feststellte und diese charakterisierte. Der Zustand von McBean verschlechterte sich im Verlaufe des Jahres 1845 rapide, er hatte starke Schmerzen und konnte das Bett nicht mehr verlassen. Am 1. Januar 1846 verstarb McBean schließlich, in seiner Todesurkunde wurde „Atrophie durch Albuminurie“ als Todesursache festgehalten.
Die Obduktion, bei der die Doktoren Macintyre, Watson und Jones anwesend waren, zeigte Knochen, die „leicht mit dem Messer zu schneiden waren und einfach brachen“. Die Rippen zerbröckelten förmlich und enthielten eine blutrote, gelatineartige und ölige Masse. Auch die gesamte Wirbelsäule war von ähnlicher Beschaffenheit. Becken-, Oberarm- und Oberschenkelknochen „widerstanden jedoch jedem Versuch, sie mit der Hand zu brechen“. Herz, Lunge und Leber wurden als weitgehend unauffällig beschrieben.John Dalrymple, Chirurg und Mitglied der mikroskopischen Fachgesellschaft, untersuchte zwei Lendenwirbel und eine Rippe von McBean. Er stellte Löcher im Knochen des Patienten fest, welche mit einer roten, gelartigen Masse gefüllt waren. Diese untersuchte er unter dem Mikroskop und fand große, gleichförmig aussehende runde bis ovale Zellen, teilweise mit mehreren Nuclei. Die nach Zeichnungen von Dalrymple angefertigten Holzschnitte zeigen die noch heute gültigen Kriterien für Myelomzellen.
Epidemiologie
Die Inzidenz des Multiplen Myeloms liegt bei etwa vier bis sechs Neuerkrankungen/100.000 Personen pro Jahr. Dies entspricht zehn Prozent aller hämatologischen Krebserkrankungen bzw. ein Prozent aller Krebserkrankungen insgesamt. Sie ist eine Erkrankung des höheren Lebensalters, wobei das mediane Alter zum Zeitpunkt der Diagnosestellung bei 66 Jahren liegt. Nur zwei Prozent der Patienten sind jünger als 40 Jahre. Bei Kindern tritt es sehr selten auf. Männer sind etwas häufiger als Frauen betroffen und bei Afroamerikanern kommt die Erkrankung im Vergleich zur weißen US-amerikanischen Bevölkerung etwa doppelt so häufig vor. Die Fünfjahresprävalenz beträgt nach aktuellen Daten weltweit für alle Altersgruppen über 350.000 Personen.
Entsprechend dem gebildeten Antikörper werden folgende Typen unterschieden:
| Monoklonales Tumorprodukt | Häufigkeit | IgG | IgA | IgM | IgD | IgE | Kappa | Lambda | ||
|---|---|---|---|---|---|---|---|---|---|---|
| Ausschließlich intaktes Immunglobulin | 5–10 % | ca. 55 %* | ca. 20 %* | ca. 0,5 %* | ca. 2 %* | extrem selten | ||||
| Freie Leichtkette mit oder ohne intaktem Immunglobulin | 90–95 % | Freie Leichtkette mit intaktem Immunglobulin | 70–75 % | 57 %* | 34 %* | |||||
| Ausschließlich freie Leichtkette | 15–20 % | |||||||||
| Nicht-sekretorisch | 1–2 % | |||||||||
| *bezogen auf die Gesamtheit der Myelom-Patienten | ||||||||||
Hervorzuheben ist, dass bei einem Myelom, bei dem ein intaktes Immunglobulin gebildet wird, z. B. bei einem IgG-Myelom, in ca. 90–95 % der Fälle auch eine freie Leichtkette in erhöhter Menge vorliegt (z. B. eine freie Leichtkette vom Typ κ bei einem IgGκ-Myelom). Bei nur 5–10 % der Fälle findet sich ausschließlich ein intaktes Immunglobulin und in wenigen Fällen scheiden die Plasmazellen kein monoklonales Immunglobulin bzw. keine freie Leichtketten aus. In diesen Fällen spricht man von einem sogenannten nicht-sekretorischen Multiplen Myelom. Monoklonale Immunglobuline werden zum Teil produziert, verbleiben aber daraufhin innerhalb der Plasmazelle und können nur durch immunhistochemische Methoden (intrazelluläre Anfärbung) nachgewiesen werden. Selten finden sich zudem Fälle, bei denen die Plasmazellen weder intakte Immunglobuline noch freie Leichtketten produzieren (sog. echtes nicht-sekretorisches Multiples Myelom).
Pathogenese
Risikofaktoren
Die pathogenetischen Ursachen des Multiplen Myeloms sind Gegenstand aktueller Forschung. Diskutiert werden Einflüsse unterschiedlicher Umweltfaktoren. So werden mit der Entstehung der Erkrankung ionisierende Strahlung, Herbizide (z. B. Glyphosat), Übergewicht, Autoimmunerkrankungen und gehäufte entzündliche Prozesse sowie Infektionen in Verbindung gebracht. Zum Teil wurden verschiedene genetische Translokationen beschrieben, deren Einfluss aber noch nicht gänzlich geklärt ist. Auch ein Zusammenhang mit der konventionellen Gasförderung oder beim Fracking entstehenden Emissionen wird vermutet.
Entwicklung
Der Übergang von einer Monoklonalen Gammopathie unklarer Signifikanz (MGUS) zum symptomatischen Myelom verläuft in mehreren Schritten und kann wenige Monate bis mehrere Jahrzehnte dauern. Die maligne Entartung der Myelom-Zellen findet meist außerhalb des Knochenmarks in Keimzentren peripherer lymphatischer Organe statt. Die B-Zellen, die in diese Keimzentren eintreten, haben schon die ersten Differenzierungschritte (V(D)J-Rekombination) hinter sich. In diesem Stadium treten die genetischen Veränderungen auf, die letztlich zur Entwicklung des Multiplen Myeloms führen.
Bei den meisten Patienten beobachtet man Translokationen, die bewirken, dass ein Onkogen unter die Kontrolle eines regulatorischen Gens gelangt und dadurch die Expression stark aktiviert wird. Beim Multiplen Myelom ist dies am häufigsten (ca. 80 %) das Immunglobulin-Enhancer-Gen auf Chromosom 14 Genlocus q31. Häufige Partner dieser Translokation sind Teile der Chromosomen 4 (4p16.3; Fibroblast Growth Factor Receptor), 6 (6p21; Cyclin D3), 11 (Bcl-1, Cycin D1), 16 (16q23; C-maf) und 20 (20p11; maf8). Selten findet man 8q24 (c-myc) und noch seltener 18q21 (bcl-2), 11q23 (MLL-1) sowie 20q11 (maf B). Im weiteren Verlauf der Erkrankung treten noch andere genetische Veränderungen auf. Die verschiedenen genetischen Veränderungen gehen mit unterschiedlichen Krankheitsverläufen einher und definieren unter Umständen eigene Entitäten. Durch den Nachweis bestimmter genetischer Veränderungen in Myelom-Zellen eines Patienten können in manchen Fällen Aussagen zur Prognose gemacht werden. So weiß man beispielsweise, dass eine Deletion (del13q) oder eine Monosomie von Chromosom 13 im Mittel mit einer kürzeren Überlebenszeit verbunden sind. Nach der klonalen Vermehrung einer entarteten Plasmazelle kommt es zur Infiltration des Knochenmarks u. U. auch mit begleitender Zerstörung des Knochens und Verdrängung der normalen Hämatopoese (Blutbildung). Hierbei scheiden die malignen Zellen Wachstumsfaktoren und Zytokine aus, welche die Osteoklasten aktivieren (u. a. OAF), was letztlich zu einem Knochenabbau führt. Die von den malignen Zellen gebildeten Antikörper oder Antikörperteile (freie Leichtketten oder Bruchstücke der schweren Kette), welche sich im Körper anreichern, sind für einige Symptome und Komplikationen der Erkrankung verantwortlich.
Symptome
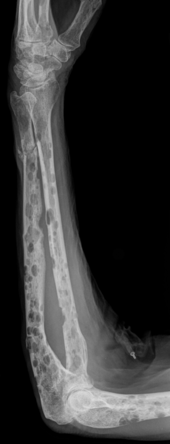
Bei einigen Patienten wird die Erkrankung zufällig im Rahmen einer Blutuntersuchung anhand einer auffälligen Serumproteinelektrophorese diagnostiziert. Bei den meisten Patienten treten jedoch Symptome und Komplikationen auf:
- Unspezifische Symptome wie Schwäche, Müdigkeit und Gewichtsverlust
- Insgesamt entwickeln etwa 60 % der Patienten Knochenveränderungen:
- Starker Knochenabbau/-schäden durch Osteolyse (die Schäden wirken im Gegensatz zu Knochenmetastasen wie ausgestanzt – typisch: Schrotschussschädel)
- Durch die Osteolyse bedingte sekundäre Osteoporose (nicht zu verwechseln mit der primären Form)
- Durch die Osteolyse bedingte Knochenschmerzen und Knochenbrüche
- Verminderung der Knochenmarksfunktion (Knochenmarkinsuffizienz) mit Blutarmut (Anämie) und Neigung zu Blutungen sowie Verminderung der weißen Blutkörperchen (Leukopenie) und/oder der Blutplättchen (Thrombozytopenie) mit Neigung zur Thromboembolie
- Infektanfälligkeit durch Mangel polyklonaler Antikörper und Mangel an weißen Blutkörperchen (Leukopenie)
- Erhöhte Viskosität des Serums durch monoklonale Immunglobuline kann zu Kopfschmerzen, Benommenheit, Schwindel, Nystagmus, Hör- und Sehstörungen, Schläfrigkeit, Koma und Krampfanfällen führen (Hyperviskositätssyndrom)
- Unter Umständen Ablagerungen monoklonaler Immunglobuline oder freier Leichtketten im peripheren Nervensystem (Polyneuropathie)
-
Chronisches oder akutes Nierenversagen. Ist die Störung der Nierenfunktion auf eine monoklonale freie Leichtkette oder ein monoklonales intaktes Immunglobulin zurückzuführen, kann von einer Monoklonalen Gammopathie renaler Signifikanz gesprochen werden. Beispiele sind (Auswahl):
- Cast-Nephropathie: In den Nierenkanälchen kann es in Gegenwart von Uromodulin zu Ausfällungen der freien Leichtketten in Form von Eiweißzylindern kommen. Diese Ausfällungen wirken direkt toxisch auf die Zellen der Nierenkanälchen und können zu einem raschen Verlust der Nierenfunktion (akutes Nierenversagen) führen (klassische Myelomniere; auch als Cast-Nephropathie bekannt).
- Leichtketten-Ablagerungs-Krankheit: Ablagerung von Leichtketten in den Basalmembranen von Nierenkörperchen und Nierenkanälchen kann zur Leichtketten-Ablagerungs-Krankheit (light-chain deposition disease) führen. Diese äußert sich in einer stark vermehrten Ausscheidung von Eiweiß im Urin (nephrotisches Syndrom) und führt zu chronischem Nierenversagen.
- Fanconi-Syndrom: Die Leichtketten können zu Funktionsstörungen der Zellen im Hauptstück der Nierenkanälchen führen. Diese Funktionsstörungen äußern sich in einer verminderten Ausscheidung von Säuren (Azidose) sowie einem vermehrten Verlust von Phosphat, Glukose, Harnsäure und Aminosäuren.
- AL-Amyloidose: Durch Fehlfaltung freier Leichtketten kommt es zur Bildung von Fibrillen, die sich in Form von Amyloiden in Nierengewebe und Nierengefäßen ablagern. Folge sind wie bei der Leichtketten-Ablagerungs-Krankheit erhöhte Proteinurie und ein chronisches Nierenversagen.
Die typische aber zugleich auch unspezifische Symptomatik erschwert eine eindeutige Diagnose. Viele der hier beschriebenen Symptome können auch in einem früheren Krankheitszustand auftreten und müssen sich nicht zwangsläufig erst bei einem per Definition Multiplen Myelom ausbilden. Eine umfassende Anamnese des Patienten ermöglicht eine sichere Diagnose der zugrundeliegenden Erkrankung. Unter Patienten mit bekannten Vorerkrankungen, wie Osteoporose oder Polyneuropathie, kann mit einer erhöhten Wahrscheinlichkeit eine Monoklonale Gammopathie wie das Multiple Myelom vorliegen. Im nächsten Abschnitt sind die aktuell gültigen Empfehlungen zur Diagnose und die diagnostischen Kriterien zusammengefasst.
Diagnose
Diagnostische Kriterien
Als Grundvoraussetzung gilt eine ≥10%ige Infiltration des Knochenmarks durch klonale Plasmazellen oder ein durch Biopsie bestätigtes extramedulläres Plasmozytom. Wird zusätzlich eines oder mehrere der folgenden Kriterien erfüllt, kann die Diagnose Multiples Myelom gestellt werden:
-
CRAB-Kriterien: Calcium, Renale Insuffizienz, Anämie, Bone = Knochen
- Hyperkalzämie im Serum nachweisbar mit einem Wert von > 2,75 mmol/l oder > 0,25 mmol/l oberhalb des oberen Normwertes.
- Niereninsuffizienz, definiert als Serumkreatinin > 2 mg/dl oder einer Kreatinin-Clearance < 40 ml/min.
- Anämie, definiert als Hämoglobinwert von < 10 g/dl oder mehr als 2,0 g/dl unter dem Normwert.
- Knochenläsionen mit mindestens einer osteolytischen Läsion, nachweisbar durch Röntgen, CT oder PET-CT.
-
SLiM-Kriterien: Sixty Percent = 60 Prozent, Light chain ratio, MRT-Läsion
- ≥ 60%ige Infiltration von Plasmazellen im Knochenmark.
- eine Freie-Leichtketten-Ratio der tumorassoziierten freien Leichtkette (involvierte freie Leichtkette) zur nicht-tumorassoziierten freien Leichtkette (nicht involvierte freie Leichtkette) von ≥ 100 (wobei die tumorassoziierte freie Leichtkette mit einer Konzentration von mindestens 100 mg/l vorliegen muss).
- > 1 fokale Knochenläsion mit einer Größe von mindestens 5 mm nachgewiesen durch eine Ganzkörperaufnahme im MRT.
Differentialdiagnose
Um die Diagnose anhand der oben genannten Kriterien stellen zu können, müssen verschiedene Untersuchungen durchgeführt werden. In den hämatologischen Leitlinien finden hierbei folgende Methoden Erwähnung:
| 1. Labordiagnostik | 2. Bildgebung | 3. Untersuchung des Knochenmarks |
|---|---|---|
|
Als Standardmethoden gelten:
Außerdem:
|
|
|
Wird durch die oben genannten Untersuchungen ein positiver Befund erzielt bzw. CRAB-/SLiM-Kriterien erfüllt, sind folgende zusätzlichen Untersuchungen vor Einleitung einer Therapie in Betracht zu ziehen:
- Magnet-Resonanz-Tomographie (MRT) gezielter Regionen (ggf. mit Kontrastmittel), insbesondere bei
- neurologischer Symptomatik mit Verdacht auf Myelonkompression
- Verdacht auf extramedulläre Manifestationen
- Echokardiographie bei (v. a. kardiale Amyloidose)
Differentialdiagnostisch abzugrenzen sind neben reaktiven Knochenmarksveränderungen auch die Vorstufen SMM und MGUS siehe hierzu die allgemeinen Diagnosekriterien Monoklonaler Gammopathien.
Prognose
Viele verschiedene Faktoren spielen eine Rolle bei der Entwicklung der Krankheit und in deren Verlauf. So z. B. das Alter bei Krankheitsbeginn, die körperliche Allgemeinverfassung, das Ausmaß der begleitenden Erkrankungen, das Auftreten von Komplikationen oder unvorhergesehenen Ereignissen und/oder das Ansprechen auf die Behandlungsmaßnahmen. Die Überlebensraten haben sich innerhalb der letzten zehn Jahre laut Hartmut Goldschmidt durch die neuen Therapiemöglichkeiten (s. u.) signifikant verbessert. Sie können das Gesamtüberleben und die beschwerdefreie Zeit verlängern. Nicht zuletzt erhöhen sie die Lebensqualität von Betroffenen und Angehörigen. Zusammengefasst kann nach aktuellem Stand von einer absoluten Fünfjahresüberlebensrate von 41 % für Männer bzw. 40 % für Frauen gesprochen werden. Unter Berücksichtigung der Sterblichkeit in der Allgemeinbevölkerung liegt die relative Fünfjahresüberlebensrate aktuell bei 48 % für Männer bzw. 45 % für Frauen. Für Männer bzw. Frauen liegt die jeweilige relative Zehnjahresüberlebensrate bei 31 % bzw. 30 %. Durch eine Einteilung in Stadien sowie eine Risikostratifizierung können Patienten differenzierter beurteilt und eine genauere Prognose gestellt werden.
Stadieneinteilung
Die nach wie vor gängige Einteilung nach Brian Durie und Sydney Salmon unterscheidet drei Stadien:
| Stadium | Merkmale |
|---|---|
| Stadium I |
|
| Stadium II | zwischen Stadium I und III |
| Stadium III | mindestens eines der folgenden Kriterien:
|
| Zusatz A B |
|
Neuer ist die Einteilung nach dem International Staging System (ISS), bei der nur β2-Mikroglobulin und Albumin berücksichtigt werden.
| Stadium | Merkmale |
|---|---|
| ISS I | β2-Mikroglobulin < 3,5 mg/l und Albumin ≥ 35 g/l |
| ISS II | β2-Mikroglobulin < 3,5 mg/l und Albumin < 35 g/l oder β2-Mikroglobulin 3,5–5,5 mg/l |
| ISS III | β2-Mikroglobulin > 5,5 mg/l |
Im Jahr 2015 erfolgte eine Revision der Kriterien, wobei nun auch prognostisch relevante zytogenetische Marker sowie die LDH als Laborparameter in die Stadienzuteilung einfließen.
| Stadium | Merkmale |
|---|---|
| R-ISS I | β2-Mikroglobulin < 3,5 mg/l und Albumin ≥3,5 g/dl und Zytogenetik Standardrisiko und LDH ≤ oberer Normwert |
| R-ISS II | weder Stadium I noch Stadium III |
| R-ISS III | β2-Mikroglobulin > 5,5 mg/l und Zytogenetik Hochrisiko oder LDH > oberer Normwert |
Risikostratifizierung
Sollte bereits vor Ausbildung der Erkrankung die Vorstufe MGUS diagnostiziert worden sein, können folgende Faktoren zur Beurteilung eines Risikos zur Ausbildung eines symptomatischen Multiplen Myeloms herangezogen werden:
- abnormale Ratio der freien Leichtketten
- M-Protein im Serum > 15 g/l
- M-Protein vom Typ IgA, IgM, IgD oder IgE
Unter Berücksichtigung der durchschnittlichen Lebenserwartung kann von einem 2%igen Risiko bei Abwesenheit aller Faktoren, bei Nachweis von einem Faktor von einem 10%igem Risiko, einem 18%igen Risiko bei Nachweis von zwei Faktoren und einem 27%igem Risiko bei Nachweis von allen drei Faktoren zur Weiterentwicklung der MGUS zum Multiplen Myelom innerhalb von 20 Jahren ausgegangen werden. Werden anschließend regelmäßige Untersuchungen der betroffenen Patienten durchgeführt (je nach Risikoeinstufung alle sechs Monate, jährlich oder alle zwei bis drei Jahre) kann das Risiko von Komplikationen durch das Fortschreiten der Erkrankung bzw. Vorstufe vermindert werden.
Auf ähnliche Art und Weise können auch Patienten mit einem bereits nachgewiesenen schwelenden Multiplen Myelom anhand folgender Faktoren für ein ca. 50%iges Risiko einer Progression innerhalb von zwei Jahren eingestuft werden. Grundvoraussetzung sind mindestens 10 % klonale Plasmazellen im Knochenmark und ein oder mehrere der folgenden Kriterien:
- Anstieg des M-Proteins im Serum in zwei aufeinanderfolgenden Messungen um mindestens 25 %
- M-Protein im Serum von mindestens 30 g/l
- Ratio der tumorassozierten zur nicht tumorassoziierten freien Leichtkette mindestens 8
- SMM vom Typ IgA
- Supression zweier nicht tumorassoziierter Immunglobulin-Isotypen
- Erhöhte Zahl zirkulierender Plasmazellen
- Zytogenetische Abnormalitäten der Chromosomen 4, 14 und 17
- Nachweis durch PET-CT oder MRT von fokalen Läsionen (mindestens eine) ohne osteolytische Knochenschäden
- 50–60 % klonale Plasmazellen im Knochenmark
Eine abnormale Ratio der freien Leichtketten, ein M-Protein im Serum von mindestens 30 g/l und klonale Plasmazellen im Knochenmark von mindestens 10 % gelten als unabhängige Risikofaktoren. Nach fünf Jahren liegt das Progressionsrisiko bei Anwesenheit einer dieser Faktoren bei 25 %, bei Anwesenheit von zwei Faktoren bei 51 % und bei Anwesenheit aller drei Faktoren bei 76 %. Die empfohlenen Nachuntersuchungsintervalle sind alle zwei bis drei Monate, bei stabilen Werten im ersten Jahr nach Diagnosestellung alle vier bis sechs Monate und anschließend bei unverändert stabilen Werten alle sechs bis zwölf Monate.
Therapie
Bis zum heutigen Stand der Wissenschaft ist eine Heilung des Multiplen Myeloms nicht möglich. Regelmäßige Labortests sowie Röntgen- und Knochenmarkuntersuchungen informieren über den Verlauf der Erkrankung. Eine Einleitung der Therapie ist möglich, wenn sich Endorganschädigungen (CRAB- und SLiM-Kriterien – siehe oben) zeigen. Es gibt inzwischen zahlreiche Behandlungsmöglichkeiten, die den Erkrankungsstand über einen längeren Zeitraum stabil halten, die Beschwerden mindern und die Lebensqualität für die Betroffenen deutlich erhöhen können.
Therapie der Primärerkrankung
Betroffene können, je nach Möglichkeit und Indikation, mit Chemotherapie, Medikamenten, die das Immunsystem beeinflussen (Immunmodulatoren), und solchen, die die Knochenauflösung hemmen (Bisphosphonate), behandelt werden sowie eine Knochenmarktransplantation erhalten. Die Überlebensraten haben sich innerhalb der letzten zehn Jahre durch neue Medikamente wie Bortezomib, Carfilzomib, Ixazomib, Lenalidomid, Panobinostat, Pomalidomid und Thalidomid signifikant verbessert. Die Primärtherapie wird für jeden Patienten immer individuell festgelegt. Ganz wesentlich beeinflusst z. B. das Alter die Therapieentscheidung. Auch die körperliche Allgemeinverfassung und das Ausmaß der begleitenden Erkrankungen spielen eine große Rolle, welche Therapie als geeignet angesehen werden kann. Theoretisch kommen folgende Möglichkeiten infrage, wobei ein höheres Alter z. B. eine Stammzelltransplantation ausschließt:
Chemotherapie
Die klassische Kombinationstherapie besteht aus dem Zytostatikum Melphalan und dem Cortison-Präparat Prednison. Die Chemotherapie läuft üblicherweise in Zyklen ab. Bekannte und gefürchtete Nebenwirkungen sind Haarverlust und Übelkeit. Diese Nebenwirkungen können heute jedoch durch wirksame Medikamente gemildert oder ganz vermieden werden. Ein weiteres Chemotherapeutikum ist Bendamustin, das sich durch ein günstigeres Nebenwirkungsprofil auszeichnet.
Im Jahr 2019 wurden auch Bortezomib, Lenalidomid und Thalidomid in verschiedenen Kombinationen für die Behandlung des multiplen Myeloms evaluiert. Je nach Kombination kann wahrscheinlich eine teilweise starke Verlängerung des Gesamtüberlebens erzielt werden.
Autologe Stammzelltransplantation
Hierbei handelt es sich um die Transplantation von eigenen Stammzellen. Dabei werden Stammzellen aus dem Knochenmark des Patienten gewonnen und nach erfolgter Chemotherapie dem Patienten wieder zurückgegeben. Diese Stammzellen führen meist innerhalb von kurzer Zeit zur Regeneration der Blutbildung.
Allogene Stammzelltransplantation
Bei dieser wesentlich selteneren Methode werden Stammzellen eines fremden Spenders transplantiert. Für dieses Verfahren müssen die Patienten bestimmte Voraussetzungen mitbringen. Das blutbildende System des Empfängers wird nachhaltig zerstört, um durch die Gabe von möglichst identischen Blutstammzellen ein neues hämatopoetisches System zu schaffen, welches frei von kranken Blutzellen ist. Im Gegensatz zur autologen Übertragung besteht zwar grundsätzlich die Gefahr der Transplantat-gegen-Wirt-Reaktion (Graft-versus-Host disease), allerdings kann dieses Phänomen auch den positiven Effekt der Graft-versus-Malignom-Reaktion (Graft-versus-Malignom-Effekt) mit sich bringen. Die Patienten müssen bis zu einem Jahr Medikamente zur Unterdrückung der Abstoßungsgefahr (Immunsuppressiva) einnehmen. Die allogene Stammzelltransplantation ist neben der Hornhauttransplantation die einzige „Organtransplantation“, bei der die Immunsuppressiva nicht lebenslang eingenommen werden müssen.
Um Transplantat-gegen-Wirt Reaktionen zu behandeln oder zu vermeiden, wurde der Einsatz von mesenchymalen Stromazellen evaluiert. Mesenchymale Stromazellen verursachen jedoch nur eine geringe oder keine Veränderung bezüglich der Gesamtmortalität, der Rückkehr der malignen Erkrankung und der Inzidenz der akuten und chronischen Graft-versus-Host Reaktion bei prophylaktischen Zwecken.
Strahlentherapie
Im Gegensatz zu einer Chemotherapie wirkt eine Strahlentherapie lokal. Mit ihrer Hilfe soll die Teilungsfähigkeit der bösartigen Zellen gestoppt und dadurch das weitere Wachstum des Tumors verhindert werden. Nebenwirkungen treten lokal auf, je nach Lokalisation können z. B. Hautrötungen, Durchfall oder Übelkeit/Erbrechen auftreten.
Immunmodulation
Immunmodulierende Substanzen (IMiDs für den englischen Begriff: Immunomodulatory Imid Drugs) haben sich in den vergangenen Jahren als ausgesprochen wirksames Mittel gegen Krebserkrankungen erwiesen. Dabei wird die Ausschüttung von entzündungs- oder tumorfördernden Stoffen gehemmt. Zu den IMiDs gehören: Lenalidomid (Handelsname: Revlimid) und Thalidomid; Pomalidomid ist in den USA unter dem Handelsnamen Pomalyst auf dem Markt. In Europa wurde Pomalidomid im August 2013 mit dem Handelsnamen Imnovid zugelassen.
Anders als beispielsweise eine Chemotherapie, bei der neben der Zerstörung des Tumorgewebes die vorübergehende Beeinträchtigung der gesunden Zellen unvermeidlich ist, wirken IMiDs gezielt gegen die tumorauslösenden Prozesse. Für die Behandlung von Patienten, die mindestens eine vorausgegangene Therapie erhalten haben, wurde von der Europäischen Arzneimittelagentur (EMA) im Juli 2007 die perorale Lenalidomid-Darreichungsform (Revlimid Hartkapseln, Celgene) in Kombination mit Dexamethason zugelassen. Es wurde als sogenanntes Arzneimittel für seltene Leiden (Orphan-Arzneimittel) eingestuft. In Kombinationstherapie mit Dexamethason ist es bei Rückfällen oder Therapieversagen effektiver als eine Monotherapie mit Dexamethason. Lenalidomid verfügt neben der immunmodulierenden Wirkung über weitere Mechanismen der Tumorbekämpfung:
- Aktivierung von Immunzellen (T-Zellen und natürliche Killerzellen, die ihrerseits die Tumorzellen angreifen)
- Wachstumsstopp durch direkten Angriff auf die Tumorzellen
- Angiogenesehemmung (Hemmung der Neubildung von Blutgefäßen, welche den Tumor mit Nährstoffen versorgen)
- Unterdrückung der Freisetzung von tumorfördernden Botenstoffen
- Apoptose durch Zellzyklus-Arrest
- Hemmt Osteoklasten-Aktivierung
Proteasominhibition
Proteasomen sind Eiweißkomplexe, die das Wachstum und das Absterben der Zellen (Apoptose) regulieren. Proteasominhibitoren sind Substanzen, die die Aktivität von Proteasomen hemmen (inhibieren). Sie bewirken eine Verlangsamung des Zellwachstums und eine Beschleunigung der Apoptose. Der erste sowohl in den USA als auch in der EU zugelassene Proteasominhibitor ist Bortezomib (Handelsname: Velcade); Carfilzomib (Handelsname: Kyprolis) wurde 2015 sowohl in den USA als auch in der EU zugelassen.Ixazomib ist in der EU seit 2016 zugelassen. Als Wirkverstärker von Proteasominhibitoren ist der Histon-Deacetylase-Hemmer Panobinostat (Handelsname: Farydak) seit 2015 in der EU zur Behandlung des Multiplen Myeloms unter bestimmten Voraussetzungen zugelassen.
Biologika
Neuere Forschungen haben zur Entwicklung hochspezifischer Biologika geführt, die seit einiger Zeit für die Therapie des Multiplen Myeloms zugelassen sind. Darunter die monoklonalen Antikörper Daratumumab und Elotuzumab. Während Daratumumab spezifisch an das Glykoprotein CD38 bindet, welches auf Myelomzellen überexprimiert vorliegt, wodurch die Apoptose der Zellen ausgelöst wird, entfaltet Elotuzumab seine immunstimulatorischen Eigenschaften durch die Interaktion mit dem Oberflächenprotein SLAMF7 auf Myelomzellen.
Peptid-Wirkstoff-Konjugate
Bei der Konjugation werden pharmakologische Moleküle über einen Linker miteinander verknüpft. In dieser konjugierten Form weisen z. B. in der Onkologie verwendete Wirkstoffe eine selektive therapeutische antikanzerogene Aktivität auf und verschonen gleichzeitig Nicht-Tumor-Zellen. Das Peptid-Wirkstoff-Konjugat (PDC) Melphalanflufenamid (auch: Melphalan Flufenamid oder Melflufen) ist ein lipophiler Alkylator, wodurch seine Aufnahme in Zellen erleichtert wird. In der Zielzelle (Krebszelle) wird der aktive Metabolit (pharmakologisch aktiver Wirkstoff) freigesetzt. Seit 2022 ist Melphalan Flufenamid in Kombination mit dem Kortison Dexamethason in der EU zugelassen zur Behandlung von erwachsenen Patienten mit rezidiviertem oder refraktärem Multiplem Myelom (r/r MM), die zuvor mindestens drei andere Therapien (aus unterschiedlichen Wirkstoffgruppen) erhalten haben.
Supportivtherapie
Ergänzende (sogenannte supportive) therapeutische Maßnahmen können helfen, begleitende Symptome einzudämmen und Komplikationen vorzubeugen. Daher wurde evaluiert, ob körperliche Betätigung als Ergänzung zu der Standardtherapie Vorteile für die Patienten hat. Die Evidenz ist sehr ungewiss bezüglich des Effekts von körperlicher Betätigung auf Angst und schwere unerwünschte Ereignisse. Körperliche Betätigung verursacht eventuell nur eine geringe oder keine Veränderung bezüglich der Mortalität, der Lebensqualität und der körperlichen Funktion. Körperliche Betätigung verursacht eventuell eine schwache Verringerung von Depressionen.
Verlaufskontrolle
Anhand verschiedener Parameter kann die Effektivität einer Therapie beurteilt werden. Nachfolgend sind die aktuell gültigen Definitionen aus internationalen und nationalen Leitlinien aufgelistet, die hierbei Anwendung finden.
Remissionskriterien
| Kriterium/Status | M-Protein in SPE | M-Protein in IFE | Freie Leichtketten | Manifestation in Weichteilen | Anteil Plasmazellen im Knochenmark |
|---|---|---|---|---|---|
| stringente komplette Remission (sCR) | nicht nachweisbar in Serum und Urin | normalisierte Ratio der freien Leichtketten | keine nachweisbar | ≤ 5 %; keine klonalen Plasmazellen nachweisbar durch Immunhistochemie | |
| komplette Remission (CR) | nicht nachweisbar in Serum und Urin | keine nachweisbar | ≤ 5 % | ||
| sehr gute partielle Remission (VGPR) | mind. 90 % Reduktion im Serum und weniger als 100 mg/24h im Urin oder kein M Protein in Serum und Urin nachweisbar | nachweisbar | |||
| partielle Remission (PR) | mind. 50 % Abnahme im Serum und mind. 90 % Reduktion im Urin oder weniger als 200 mg/24h im Urin | falls M-Protein nicht bestimmbar gilt > 50 % Reduktion der Differenz aus tumorassoziierter (involvierter) und nicht-tumorassozierter (nicht-involvierter) freier Leichtkette = dFLC | > 50 % Reduktion (obligates Kriterium) | falls Anteil vor Therapie über 30 % und falls M-Protein und freie Leichtketten Ratio nicht bestimmbar gilt eine Reduktion der Infiltration um über 50 % | |
| stabile Erkrankung (SD) | keinerlei der Kriterien erfüllt | ||||
| progressive Erkrankung (PD) | mind. 25 % Anstieg im Serum und absolut mind. 0,5 g/dl und/oder mind. 25 % Anstieg im Urin oder absolut ≥ 200 mg/24h | mind. 25 % Anstieg der dFLC im Serum, absolut um mindestens 100 mg | Progress oder Neuauftreten | > 25 % Anstieg in Bezug auf den Wert zum Zeitpunkt des besten Ansprechens und absolut mind. 10 % | |
Minimale Resterkrankung (MRD)
Bei einer großen Mehrheit der Patienten ist auch nach Erreichen einer kompletten Remission mit verschiedenen Methoden eine minimale Resterkrankung (im Englischen als minimal residual disease (MRD) bezeichnet) nachweisbar. In einem solchen Fall ist der Patient dabei nicht als geheilt zu betrachten und unter Umständen kann es im späteren Verlauf zu einem Rezidiv kommen. Zwischenzeitlich etablierte Methoden zum Nachweis einer Resterkrankung sind Next-Generation-Sequencing, Durchflusszytometrie sowie MRT und PET. Neuere Studien zeigen außerdem, dass durch die serologische Bestimmung der Immunglobuline, entsprechend ihrer gebundenen Leichtkette, Aussagen über eine möglicherweise zugrundeliegende minimalen Resterkrankung getroffen werden kann - z. B. IgGκ als M-Protein im Normbereich und IgGλ als normales (polyklonales) Immunglobulin unterhalb des Normbereichs als Hinweis für eine MRD. Bei einer nachgewiesenen MRD-Negativität, ist von einem längeren progressionsfreien als auch Gesamtüberleben auszugehen. Diese Methoden sind aktuell noch kein Standard und tragen zurzeit noch nicht prädiktiv für weitere Therapieentscheidungen bei.
Selbsthilfegruppen
Für das Multiple Myelom gibt es verschiedene Selbsthilfegruppen in Deutschland. Die größte Selbsthilfegruppe ist die AMM-Online (Arbeitsgemeinschaft Multiples Myelom (Plasmozytom, Morbus Kahler) Online-Netzwerk für Patienten/-innen und Angehörige), die u. a. folgendes anbietet:
- ein umfangreiches Informationsangebot in allen Stadien der Erkrankung - vom MGUS über das schwelende Myelom (SMM) bis hin zum behandlungsbedürftigen Multiplen Myelom
- ein Patienten- und Angehörigenforum
- eine Auflistung von aktuell rekrutierenden Myelom Studien in Deutschland
- eine Übersicht aller deutschsprachigen Myelom-Selbsthilfe-Gruppen
Darüber hinaus bietet die AMM-Online einen monatlichen virtuellen Stammtisch an, bei dem sich Patienten und Angehörige austauschen können.
Literatur
- M. A. Bärtsch Aktuelle Aspekte bei der Diagnostik und Therapie des Plasmazellmyeloms. In: Deutsches Ärzteblatt. Band 142, Nr. 11, 2017, S. 800–804.
- D. Felsenberg Monoklonale Gammopathie unklarer Signifikanz (MGUS). In: Forum Sanitas. 2018, 2. Ausgabe, S. 39–41.
- Hartmut Goldschmidt: Das Multiple Myelom (Plasmozytom). Diagnose und Therapie. 2. Auflage. Unimed, Bremen 2011, ISBN 978-3-8374-1032-7.
- Robert A. Kyle, David P. Steensma: Multiple Myeloma: A History. In: James S. Malpas, Daniel E. Bergsagel, Robert E. Kyle: Myeloma: Biology and Management. Saunders, 3. Auflage, 2004, S. 99–117, ISBN 978-0-7216-0006-2.
- K. M. Kortüm Das multiple Myelom. In: Der Internist. Band 54, Nr. 8, 2013, S. 963–977.
- J. v. Rustitzky: Multiples Myelom. In: Deutsche Zeitschrift für Chirurgie.# 3, 1873, S. 162–172, Aufsatz im Volltext – auf dem Server der Bayerischen Staatsbibliothek.
- Christian Straka, Hermann Dietzfelbinger (Hrsg.): Manual Multiples Myelom. Empfehlungen zur Diagnostik, Therapie und Nachsorge. Tumorzentrum München. 5., überarbeitete Auflage. W. Zuckschwerdt Verlag, München 2017, ISBN 978-3-86371-211-2.
Weblinks
- AMM-Online. Netzwerk für Myelom-Patienten, Informationsportal mit Patientenforum
- Myelom.Online e.V. gemeinnützige bundesweit tätige Selbsthilfe- und Patientenorganisation von Patientinnen, Patienten und Angehörigen
- Offizielle Seite der International Myeloma Working Group (englisch)
- Plasmozytom / Multiples Myelom. Antworten. Hilfen. Perspektiven. (PDF; 1,17 MB) Blauer Ratgeber #22 der Deutschen Krebshilfe
- Myelom Kontaktgruppe Schweiz
- Multiples Myelom, Pathologie – Bilddatenbank Pathopic der Universität Basel; PathoPic – Anleitung (PDF; 2,2 MB)
- Patientenleitlinie Multiples Myelom, 1. Auflage, August 2022. 9. August 2022, abgerufen am 12. August 2022.
- Multiples Myelom – Eine Krebserkrankung des Knochenmarks – Patientenhandbuch (deutschsprachige Ausgabe) der International Myeloma Foundation
- Multiples Myelom – Eine Krebserkrankung des Knochenmarks – Kurze Zusammenfassung der Krankheit und Therapiemöglichkeiten (deutschsprachige Ausgabe) der International Myeloma Foundation
- Multiples Myelom – Eine Krebserkrankung des Knochenmarks - Freelite® - und Hevylite®-Serum-Assays verstehen. (deutschsprachige Ausgabe) der International Myeloma Foundation
- wikilite.com – englischsprachige Informationsseite zum biologischen Hintergrund, Diagnostik, Verlaufskontrolle und Therapie Monoklonaler Gammopathien
- The Myeloma Beacon englischsprachige Seite mit aktuellen Informationen zum Multiplen Myelom
- Operative Therapienotwendigkeit beim Multiplen Myelom




