
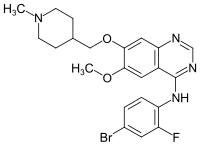
Vandetanib
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Vandetanib | |||||||||||||||||||||
| Andere Namen |
|
|||||||||||||||||||||
| Summenformel | C22H24BrFN4O2 | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 475,36 g·mol−1 | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Vandetanib, das unter dem Markennamen Caprelsa vertrieben wird, ist ein Krebsmedikament, das zur Behandlung bestimmter Tumoren der Schilddrüse eingesetzt wird. Es wirkt als Kinase-Inhibitor einer Reihe von Zellrezeptoren, hauptsächlich des vaskulären endothelialen Wachstumsfaktor-Rezeptors (VEGFR), des EGF-Rezeptors und der RET-Tyrosin-Kinase.
Das Medikament wurde von AstraZeneca entwickelt, die 2015 die Rechte an Sanofi Genzyme verkauften.
Inhaltsverzeichnis
Entwicklung und Vermarktung
Vandetanib wurde im April 2011 von der FDA für die Behandlung von Schilddrüsenkrebs im Spätstadium zugelassen und wurde zunächst ohne Handelsnamen vermarktet; seit August 2011 wird es unter dem Handelsnamen Caprelsa vermarktet. Im Februar 2012 folgte die bedingte Zulassung in der EU.
Im Jahr 2015 erwarb Sanofi Genzyme das Produkt von AstraZeneca.
AstraZeneca testete Vandetanib auch in der Kombinationstherapie des nicht-kleinzelligen Lungenkrebs in klinischen Studien. Einen im Juni 2009 gestellten Zulassungsantrag bei der EMA zog AstraZeneca jedoch vier Monate später zurück, da die Studien keinen ausreichenden Nutzen gezeigt hatten. Die Ergebnisse einer prospektiven, randomisierten, doppelblinden, multizentrischen Phase-2-Studie, die 2017 veröffentlicht wurde, zeigten keine Verbesserung im Gesamtüberleben bei lokal fortgeschrittenem oder metastasiertem Pankreaskarzinom, wenn die Patienten zusätzlich zu Gemcitabin auch Vandetanib erhielten.
Pharmakologie
Vandetanib ist ein Inhibitor von vaskulärem endothelialen Wachstumsfaktor-Rezeptor-2, epidermalem Wachstumsfaktor-Rezeptor und RET-Tyrosinkinasen. Es hemmt VEGFR-3 schwach.
Nach oraler Gabe wird Vandetanib gut aus dem Darm resorbiert, erreicht 4 bis 10 Stunden nach der Anwendung maximale Blutplasmakonzentrationen und hat eine Halbwertszeit von durchschnittlich 19 Tagen. Es muss etwa drei Monate lang eingenommen werden, um eine Steady-State-Konzentration zu erreichen. Im Blut ist es fast vollständig (90–96 %) an Plasmaproteine wie Albumin gebunden. Es wird über CYP3A4 zu N-Desmethylvandetanib und über FMO1 und 3 zu Vandetanib-N-Oxid metabolisiert. Dies sind beides aktive Metaboliten. Vandetanib wird über die Fäzes (44 %) und den Urin (25 %) in Form von unverändertem Wirkstoff und der Metaboliten ausgeschieden.
Anwendungsbeschränkungen
Nicht angewendet werden darf Vandetanib bei einem QTc-Intervall über 480 Millisekunden oder beim Vorliegen eines kongenitalen Long-QTc-Syndroms, ferner nicht gemeinsam mit Arzneimitteln, die bekanntermaßen ebenfalls das QTc-Intervall verlängern und/oder Torsade de pointes auslösen.
Nicht empfohlen wird die Verwendung von Vandetanib bei Patienten mit mittelschwerer und schwerer Leberfunktionsstörung, da die Sicherheit und Wirksamkeit noch nicht nachgewiesen ist.
Im Januar 2023 wurde durch einen Rote-Hand-Brief mitgeteilt, dass Vandetanib nicht bei Patienten angewendet werden sollte, deren RET-Mutationsstatus (Rearranged-during-Transfection-Mutation, V804M-Mutation im RET-Gen) unklar oder negativ ist. Bei diesen Patienten hat Vandetanib möglicherweise einen geringeren Nutzen. Falls solche Patienten bereits mit Vandetanib behandelt werden, empfiehlt der Hersteller, die Behandlung abzubrechen.
Nebenwirkungen
Sehr häufige (bei mehr als 10 % der Behandelten) unerwünschte Wirkungen sind Erkältungen, Bronchitis, Infektionen der oberen Atemwege, Harnwegsinfektionen, verminderter Appetit, geringe Kalziumabsorption, Schlaflosigkeit, depressive Stimmung, Kopfschmerzen, Kribbeln, seltsame, schmerzhafte Empfindungen, Schwindel, verschwommenes Sehen, Hornhautschäden, QT-Syndrom, Bluthochdruck, Magenschmerzen, Durchfall, Übelkeit, Erbrechen, Verdauungsstörungen, Photoallergische Dermatitis, Hautausschlag, Akne, trockene und juckende Haut, Nagelstörungen, Eiweiß im Urin, Nierensteine, Schwäche, Müdigkeit, Schmerzen und Ödeme.
Häufige (bei 1 % bis 10 % der Behandelten) unerwünschte Wirkungen sind Lungenentzündung, Sepsis, Grippe, Blasenentzündung, Nasennebenhöhlenentzündung, Kehlkopfentzündung, Follikulitis, Furunkel, Pilzinfektionen, Niereninfektionen, niedrige Schilddrüsenhormonwerte, niedrige Kaliumwerte, hohe Kalziumwerte, Hyperglykämie, Dehydrierung, niedrige Natriumwerte, Angstzustände, Zittern, Lethargie, Bewusstseinsverlust, Gleichgewichtsstörungen, Veränderungen des Geschmackssinns, Sehstörungen, wahrgenommene Lichtblitze, Glaukom, Konjunktivitis, trockenes Auge, Keratopathie, hypertensive Krise, Mini-Schlaganfälle, Nasenbluten, Bluthusten, Blut im Stuhlgang, Kolitis, Mundtrockenheit, Stomatitis, Verstopfung, Gastritis, Gallensteine, Hand-Fuß-Syndrom, Haarausfall, schmerzhaftes Wasserlassen, blutiger Urin, Nierenversagen, häufiges Wasserlassen, dringender Harndrang und Fieber.
Wechselwirkungen
Vandetanib wurde als Substrat für die Transporter OATP1B1 und OATP1B3 beschrieben. Die Interaktion von Vandetanib mit OATP1B1 und OATP1B3 kann seine hepatische Disposition verändern und zu Transporter-vermittelten Arzneimittelwechselwirkungen führen. Außerdem ist Vandetanib ein Inhibitor des OATP1B3-Transporters, aber nicht für OATP1B1.
Andere Arzneimittel, die das QT-Intervall verlängern, können diese Nebenwirkung von Vandetanib möglicherweise noch verstärken. Da das Medikament teilweise über das Leberenzym CYP3A4 verstoffwechselt wird, können starke Induktoren dieses Enzyms die Blutplasmakonzentrationen von Vandetanib verringern. CYP3A4-Inhibitoren erhöhen die Vandetanib-Konzentrationen nicht signifikant, vermutlich weil es auch über die flavinhaltige Monooxygenase 1 (FMO1) und 3 verstoffwechselt wird.
