Alkaloide
Alkaloide (Wortbildung aus arabisch القلية, DMG al-qalya ‚die Pflanzenasche‘ und griechisch -oides: „ähnlich“) sind natürlich vorkommende, chemisch heterogene, meist alkalische, stickstoffhaltige organische Verbindungen des Sekundärstoffwechsels, die auf den tierischen, also auch menschlichen Organismus wirken.
Über 10.000 verschiedene pflanzliche, tierische oder von Mikroorganismen produzierte Substanzen werden dieser Stoffgruppe zugeordnet. Der Begriff wurde 1819 zuerst für „alkaliähnliche“ Pflanzenstoffe wie Morphin, Strychnin und Solanin verwendet. Eine zufriedenstellende und allgemein akzeptierte Definition für den Begriff „Alkaloid“ existiert jedoch bis heute nicht.
Inhaltsverzeichnis
Definitionen
Der Begriff Alkaloid war ursprünglich eine allgemeine Bezeichnung für aus Pflanzen isolierte basische Stoffe. Später wurden Alkaloide auch aus anderen Organismen, wie Pilzen (z. B. Mutterkornalkaloide) und Tieren (z. B. das Krötenalkaloid Bufotenin) isoliert, sodass die Definition erweitert wurde. Des Weiteren wurde der Alkaloidbegriff teilweise auch auf einige nicht basische Naturstoffe, wie das Herbstzeitlosen-Alkaloid Colchicin, das Capsaicin des Cayennepfeffers oder die Purin-Alkaloide Coffein, Theophyllin und Theobromin, ausgedehnt.
Alle Alkaloide wirken charakteristisch auf den tierischen und menschlichen Organismus. Die meisten sind giftig und haben einen bitteren Geschmack. Die Basizität ist ein häufiges, aber nicht essenzielles Merkmal dieser Substanzgruppe. Basische Antibiotika, wie beispielsweise Streptomycin, die auf Mikroorganismen wirken, werden in der Regel nicht als Alkaloide bezeichnet. Darüber hinaus sind alle Alkaloide Produkte des Sekundärstoffwechsels. Sie werden für den Grundstoffwechsel der sie bildenden Organismen nicht benötigt, sondern dienen häufig als Schutz vor Fressfeinden. Basische Aminosäuren oder Peptide, die Primärstoffwechselprodukte sind, werden daher nicht den Alkaloiden zugeordnet.
Einige strenge Definitionen fordern, dass der Stickstoff Teil eines heterocyclischen, biogenetisch von Aminosäuren abgeleiteten Systems ist. Diese Definition gliedert beispielsweise die Protoalkaloide Ephedrin und Mescalin sowie die Pseudoalkaloide Coniin und Coffein aus der Familie der Alkaloide aus. Auch Atropin ist als künstliches Racemisierungsprodukt des (S)-Hyoscyamins nach strenger Auslegung kein Alkaloid.
Geschichte
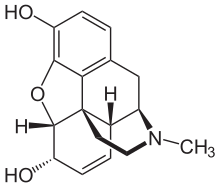
Das erste isolierte Alkaloid war Morphin, das Friedrich Wilhelm Sertürner 1804 in Reinform aus Schlafmohn extrahierte. Das Kunstwort „Alkaloide“ führte 1819 der Hallenser Apotheker Carl Friedrich Wilhelm Meißner ein. Mit der industriellen Produktion von Alkaloiden begann Emanuel Merck 1827 in Darmstadt. 1885 gelang dem Chemiker August Wilhelm von Hofmann erstmals die Strukturaufklärung und Synthese eines Alkaloids, des Coniins.
Einteilung
Alkaloide können nach verschiedenen Kriterien unterteilt werden. Üblich sind Kategorisierungen nach chemischer Struktur, Herkunft, Biogenese und pharmakologischer Wirkung.
Einteilung nach chemischer Struktur
Die in der Literatur am häufigsten verwendete Einteilung der Alkaloide ist die Kategorisierung entsprechend ihrer chemischen Struktur. Namensgebend ist der Teil des Moleküls, der das Stickstoffatom enthält.
- Alkaloide mit heterocyclischem Stickstoff
- Pyrrolidin-Alkaloide: z. B. Hygrin
- Pyrrolizidin-Alkaloide: z. B. Senezionin
- Steroid-Alkaloide: z. B. Solanin
- Pyridin-Alkaloide: z. B. Nicotin, Anabasin
- Piperidin-Alkaloide: z. B. Piperin
- Tropan-Alkaloide: z. B. Hyoscyamin, Scopolamin, Kokain
- Chinolin-Alkaloide: z. B. Chinin, Chinidin
- Isochinolin-Alkaloide: z. B. Morphin, Codein, Papaverin, Berberin, Tubocurarin
- Indolalkaloide: z. B. Ajmalin, Ergotamin, Yohimbin, Reserpin, Strychnin
- Purinalkaloide: z. B. Coffein, Theophyllin, Theobromin
- Imidazolalkaloide: z. B. Pilocarpin, Cynodin, Cynometrin, Odilin
- Acridon-Alkaloide: z. B. Acronycin, Melicopicin, Rutacridon
- Chinolizidin-Alkaloide: z. B. Lupinin, Spartein
- Benzylisochinolinalkaloide: z. B. Papaverin, Reticulin, Laudanosin
- Alkaloide mit acyclischem Stickstoff: z. B. Ephedrin, Mescalin
Einteilung nach Herkunft
Alkaloide können auch nach charakteristischen Organismen, die sie produzieren, oder nach Drogen, in denen sie enthalten sind, benannt und eingeteilt werden.
- Curare-Alkaloide: z. B. Toxiferin, Tubocurarin, Alcuronium
- Mutterkorn-Alkaloide: z. B. Ergotamin, Ergometrin
- Opiate: z. B. Morphin, Codein, Thebain, Papaverin, Noscapin, Cryptopin
- Vinca-Alkaloide: z. B. Vincristin, Vinblastin
- Lobelia-Alkaloide: z. B. Lobelin, Lelobanidin, Lobelanidin
- Strychnos-Alkaloide: z. B. Akuammicin, Brucin, Strychnin
- Catharanthus-Alkaloide: z. B. Catharanthin, Vindolin
- Amaryllidaceen-Alkaloide: z. B. Lycorin, Galantamin
- Dendrobates-Alkaloide: z. B. Histrionicotoxin, Pumiliotoxin A, Pumiliotoxin B
- Lupinen-Alkaloide: z. B. Lupinin, Lupanin, Spartein
- China-Alkaloide: z. B. Chinin, Chinidin
- Coca-Alkaloide: z. B. Cocain, Ecgonin, Hygrin
Einteilung nach Biogenese
Eine weitere Einteilung der Alkaloide kann anhand von Gemeinsamkeiten und Unterschieden der Biosynthese erfolgen. Dabei werden Alkaloide entsprechend den Aminosäuren geordnet, die als Stickstoffquelle in der Biosynthese genutzt werden.
- Von Asparaginsäure oder Lysin abgeleitete Alkaloide: z. B. Nicotin, Lupinin
- Von Glycin abgeleitete Alkaloide: z. B. Coffein, Theophyllin, Theobromin
- Von Histidin abgeleitete Alkaloide: z. B. Pilocarpin
- Von Ornithin abgeleitete Alkaloide: z. B. Hyoscyamin, Scopolamin, Kokain
- Von Phenylalanin oder Tyrosin abgeleitete Alkaloide: z. B. Colchicin, Morphin, Codein, Papaverin, Tubocurarin, Berberin
- Von Tryptophan abgeleitete Alkaloide: z. B. Ergotamin, Ergometrin, Ajmalin, Reserpin, Strychnin
Demgegenüber weist der Sammelbegriff Terpenalkaloide, zu denen beispielsweise das Diterpenalkaloid Aconitin und die Steroidalkaloide zählen, auf die biogenetische Herkunft des Kohlenstoffgrundgerüstes aus dem Terpenstoffwechsel hin.
Einteilung nach pharmakologischer Wirkung
- Nach pharmakologischer Wirkung; z. B. Halluzinogene
Gewinnung
Die im biologischen Material hauptsächlich in Form ihrer Essig-, Oxal-, Milch-, Wein-, Aconit- oder Chinasäure-Salze, seltener in Reinform oder als Ester vorliegenden Alkaloide werden auf klassische Weise durch Extraktion gewonnen. Das Verfahren der Extraktion hängt von den physikochemischen Eigenschaften der zu isolierenden Alkaloide ab. Für die meisten Alkaloide hat sich die Verwendung des polaren Lösungsmittels Methanol unter Zusatz von Essigsäure bewährt. Nach Eindampfen und Aufnahme in einem wässrigen sauren Medium (z. B. verdünnte Salzsäure) können Fremdbestandteile, wie Fette und andere lipophile Stoffe, durch Extraktion mit dem lipophilen Lösungsmittel Ether entfernt werden. Für die Extraktion der Alkaloide aus der wässrigen Phase hat sich Chloroform nach Alkalisierung mit Natronlauge oder einer anderen geeigneten Base bewährt. Aus der Chloroformphase geht nach Trocknen und Eindampfen in der Regel ein Alkaloidgemisch hervor, das bevorzugt durch Chromatographie aufgetrennt werden kann. Zur Isolierung lipidunlöslicher Alkaloide mit einer quartären Ammoniumstruktur kann eine Fällung mit Pikrin- oder Reineckesäure dienen.
Zudem ist für zahlreiche Alkaloide eine Partialsynthese oder chemische Totalsynthese möglich. Diese wendet man insbesondere an, wenn sie preisgünstiger als die Extraktion sind. Ein Beispiel für üblicherweise synthetisch hergestellte Alkaloide ist Theophyllin.
Analytik
Als klassisches Nachweisreagenz für Alkaloide wird Dragendorff-Reagenz verwendet. In Gegenwart von Alkaloiden bildet es ein Ionenpaar mit der Zusammensetzung [BiI4]−[NHR3]+, das, je nach Alkaloid, als gelboranges bis braunes Präzipitat zu erkennen ist. Alternativ dazu werden auch Mayers Reagenz (Tetraiodomercurat), Silicowolframsäure, Wagners Reagenz (Iod-Kaliumiodid), Sonnenscheins Reagenz (Phosphomolybdänsäure), Iodoplatinat und weitere als Nachweisreagenz verwendet. Die Selektivität dieser Nachweisreagenzien variiert stark und ist innerhalb der Gruppe der Alkaloide begrenzt. Um die Selektivität zu erhöhen, kombiniert man sie in der Regel mit chromatographischen Verfahren wie der Dünnschichtchromatographie.
Literatur
- Jürgen Müller: Die Konstitutionserforschung der Alkaloide: Die Pyridin-Piperidin-Gruppe. Deutscher Apotheker Verlag, 1998, ISBN 3-7692-0899-4.
- Eberhard Breitmaier: Alkaloide. Betäubungsmittel, Halluzinogene und andere Wirkstoffe, Leitstrukturen aus der Natur. 3. Auflage. Vieweg + Teubner Verlag, Wiesbaden 2008, ISBN 978-3-8348-0531-7.
- Waltraud Stammel, Helmut Thomas: Endogene Alkaloide in Säugetieren. Ein Beitrag zur Pharmakologie von körpereigenen Neurotoxinen. In: Naturwissenschaftliche Rundschau. Band 60, Nr. 3, 2007, S. 117–124.
- Manfred Hesse: Alkaloide. Fluch oder Segen der Natur? Verlag Helvetica Chimica Acta, Zürich 2000, ISBN 3-906390-19-5.
- Wolf-Dieter Müller-Jahncke: Alkaloide. In: Werner E. Gerabek, Bernhard D. Haage, Gundolf Keil, Wolfgang Wegner (Hrsg.): Enzyklopädie Medizingeschichte. de Gruyter, Berlin/ New York 2005, ISBN 3-11-015714-4, S. 39.
Weblinks
- Biosynthese der Alkaloide (Memento vom 22. April 2009 im Internet Archive)