
Dichlormethan
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| |||||||||||||||||||
| Keilstrichformel zur Verdeutlichung der Geometrie | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Dichlormethan | ||||||||||||||||||
| Andere Namen | |||||||||||||||||||
| Summenformel | CH2Cl2 | ||||||||||||||||||
| Kurzbeschreibung |
farblose Flüssigkeit mit süßlichem Geruch |
||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 84,93 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig |
||||||||||||||||||
| Dichte |
1,33 g·cm−3 (20 °C) |
||||||||||||||||||
| Schmelzpunkt |
−97 °C |
||||||||||||||||||
| Siedepunkt |
40 °C |
||||||||||||||||||
| Dampfdruck |
|
||||||||||||||||||
| Löslichkeit |
wenig in Wasser (20 g·l−1 bei 20 °C) |
||||||||||||||||||
| Dipolmoment |
1.62 D |
||||||||||||||||||
| Brechungsindex |
1,4242 (20 °C) |
||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| MAK |
Schweiz: 50 ml·m−3 bzw. 180 mg·m−3 |
||||||||||||||||||
| Treibhauspotential |
11 (bezogen auf 100 Jahre) |
||||||||||||||||||
| Thermodynamische Eigenschaften | |||||||||||||||||||
| ΔHf0 |
|
||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||
Dichlormethan (DCM, auch Methylenchlorid) ist eine organische chemische Verbindung aus der Gruppe der Chlorkohlenwasserstoffe mit der Summenformel CH2Cl2. Im Vergleich zur Stammverbindung Methan sind zwei Wasserstoff- durch Chloratome substituiert.
Inhaltsverzeichnis
Darstellung und Gewinnung
Großtechnisch wird Dichlormethan in einer radikalischen Substitution durch direkte Reaktion von Methan oder Chlormethan mit Chlor bei einer Temperatur von 400–500 °C hergestellt. Bei dieser Temperatur findet eine schrittweise radikalische Substitution bis hin zu Tetrachlormethan statt:
- Methan reagiert mit Chlor unter Bildung von Chlorwasserstoff zu Chlormethan, weiter zu Dichlormethan, Trichlormethan und schließlich Tetrachlormethan.
Das Ergebnis des Prozesses ist eine Mischung der vier Chlormethane, die durch Destillation getrennt werden können.
Dichlormethan kann durch Rückflusskochen über Phosphorpentoxid (oder Phosphorpentoxid-haltigen Trocknungsmitteln) und anschließende Destillation getrocknet werden. Die Aufbewahrung von getrocknetem Dichlormethan erfolgt über ein Molekularsieb 3 Å = 0,3 nm.
Eigenschaften
Physikalische Eigenschaften
Dichlormethan ist eine farblose, nur schwer brennbare Flüssigkeit mit einem Schmelzpunkt von −96,7 °C. Der Siedepunkt bei Normaldruck liegt bei 39,8 °C. Die Verdampfungsenthalpie beträgt 28,82 kJ/mol. Die Dampfdruckfunktion ergibt sich nach Antoine entsprechend log10(P) = A−(B/(T+C)) (P in bar, T in K) mit A = 4,53691, B = 1327,016 und C = −20,474 im Temperaturbereich von 233 bis 313 K. Es riecht süßlich, ähnlich dem Chloroform. Die Mischbarkeit mit Wasser ist begrenzt. Mit steigender Temperatur sinkt die Löslichkeit von Dichlormethan in Wasser bzw. steigt die Löslichkeit von Wasser in Dichlormethan.
| Löslichkeiten zwischen Dichlormethan und Wasser | ||||||||||||
| Temperatur | °C | 0 | 9,2 | 17,3 | 26,8 | 35,7 | ||||||
| Dichlormethan in Wasser | in Ma-% | 2,03 | 1,92 | 1,80 | 1,72 | 1,77 | ||||||
| Wasser in Dichlormethan | in Ma-% | 0,082 | 0,106 | 0,135 | 0,186 | 0,218 | ||||||
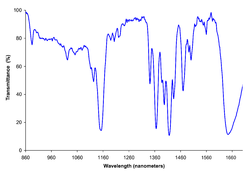
Sicherheitstechnische Kenngrößen
Dichlormethan kann entzündliche Dampf-Luft-Gemische bilden. Der Explosionsbereich liegt zwischen 13 Vol.‑% (450 g/m³) als untere Explosionsgrenze (UEG) und 22 Vol.‑% (780 g/m³) als obere Explosionsgrenze (OEG). Der untere Explosionspunkt liegt bei −8 °C. Der maximale Explosionsdruck beträgt 5,9 bar. Die Verbindung lässt sich allerdings nur sehr schwer entzünden. Das zeigt sich in der sehr hohen Mindestzündenergie von 9300 mJ. Es konnte deshalb auch kein Flammpunkt in Luft gemessen werden. In reinem Sauerstoff wird ein Flammpunkt bei −7 °C beobachtet. Die Zündtemperatur beträgt 605 °C. Der Stoff fällt somit in die Temperaturklasse T1. Die elektrische Leitfähigkeit ist mit 4,3·10−9 S·m−1 eher gering.
Verwendung
Das leicht flüchtige Dichlormethan löst viele organische Substanzen und wird beispielsweise als Lösungsmittel für Harze, Fette, Kunststoffe und Bitumen eingesetzt.
Dichlormethan dient als Abbeizmittel für Lacke, Entfettungsmittel, Treibgas für Aerosole, Treibmittel bei der Herstellung von Schaumstoffen, Kältemittel in Kühlaggregaten sowie als Extraktionsmittel für Koffein, Hopfenextrakte und Aromastoffe.
Beim Herstellen von Polyurethanschäumen hat es lange Zeit das ungiftige, aber ozonabbauende Kältemittel 1,2-Dichlor-1-fluorethan (R-141) ersetzt. Aufgrund des Substitutionsgebotes werden heutzutage in Europa die meisten Polyurethanhartschäume mit Wasser oder Pentan/Cyclopentan aufgeschäumt.
In der laborchemischen Synthese ist Dichlormethan eines der gängigsten Lösungsmittel bei Reaktionen und Extraktionen und wird oft als Ersatz für das teurere und bereits an Luft und Licht zu Phosgenbildung neigende Chloroform genommen.
Im Modellbau (z. B. Architektur) wird es aufgrund seiner Fähigkeit, Acrylglas transparent und schnell zu verbinden, ohne die Finger zu verkleben, häufig als Klebstoff eingesetzt. Auch für Polystyrol kommt es im Modellbau zur Anwendung.
In der Industrie wird Dichlormethan ebenfalls häufig dazu verwendet, Kunststoffe anzulösen und dadurch zu kleben. Dazu gehört eine Vielzahl thermoplastischer Kunststoffe wie Polystyrol, Acrylglas, Polycarbonat, Polyethylenterephthalat und Acrylnitril-Butadien-Styrol. Polypropylen und Polyethylen lassen sich mit Dichlormethan nicht kleben, weil diese nicht löslich sind.
Dichlormethan wird im „Direkten Verfahren“ zur Entkoffeinierung von Kaffee verwendet.
Aufgrund seines niedrigen Siedepunkts kann Dichlormethan in Wärmekraftmaschinen eingesetzt werden, um aus geringen Temperaturunterschieden Bewegungsenergie zu erzeugen. Ein Beispiel ist der Trinkvogel.
Dichlormethan-d2
Vollständig deuteriertes Dichlormethan (Dichlormethan-d2) – in dem beide Wasserstoffatome durch Deuterium ausgetauscht sind – wird als Lösungsmittel in der NMR-Spektroskopie benutzt.
Sicherheitshinweise
Dichlormethan ist weniger toxisch als andere einfache Organochlorverbindungen. Durch seine hohe Flüchtigkeit ist es jedoch ein gefährliches Atemgift.
Bei Aufnahme von flüssigem Dichlormethan – auch über die Haut – treten Vergiftungserscheinungen wie Kopfschmerzen, Schwindel, Übelkeit, Gefühlslosigkeit, Reizungen der Atemwege und Augen, Appetitlosigkeit, Konzentrationsschwäche und Ermüdung bis hin zu narkoseähnlichen Zuständen und Asphyxie auf.
Dichlormethan wird im Körper zu Kohlenstoffmonoxid umgesetzt und kann zur Kohlenmonoxid-Vergiftung führen.
Die Inhalation kann zur Schädigung des Sehnervs führen und Hepatitis auslösen. Längerer Hautkontakt führt zur Auflösung des Fettgewebes in der Haut und verursacht Juckreiz sowie Verätzung.
Die Dämpfe sind schwerer als Luft. Bei der Verbrennung von Dichlormethan kann das gasförmige, hochgiftige Phosgen entstehen. In Wasser gelöst schädigt es Kleinorganismen wie Daphnien.
Für Dichlormethan besteht der Verdacht auf krebserzeugende Wirkung. In Versuchstieren entstand Krebs in den Lungen, der Leber, der Bauchspeicheldrüse, im Brustdrüsengewebe und in der Speicheldrüse. Dichlormethan tritt auch in die Plazenta über.
Bei bestehenden Herzproblemen können Herzrhythmusstörungen und Herzinfarkte ausgelöst werden. Beim Umgang mit Dichlormethan sollte Schutzkleidung einschließlich Handschuhen getragen werden. Latex- oder Nitrilhandschuhe sind nicht ausreichend. Stattdessen sollten Handschuhe aus Viton oder PVA verwendet werden. Butylhandschuhe sollten jedoch nur als Spritzschutz eingesetzt werden, da die Durchbruchzeit bei 8 Minuten liegt. Die Lagerung dieser Verbindung sollte in einem Temperaturbereich von 15 bis 25 °C erfolgen. Dichlormethan darf keinesfalls mit metallischem Natrium oder anderen Alkalimetallen in Kontakt kommen, weil dies zu Explosionen führen kann.
Rechtliche Situation
Die Verwendung von Dichlormethan in Abbeizmitteln wurde durch den Beschluss 455/2009/EG des Europäischen Parlamentes am 6. Mai 2009 für Privatpersonen sowie die gewerbliche Verwendung verboten. Ausgenommen hiervon bleibt die Industrie. Vorausgegangen war diesem Schritt die Richtlinie 76/769/EWG, die durch den Neubeschluss in Anhang XVII der REACH-Verordnung übernommen wurde. Voraussetzung dieser Richtlinie war in Deutschland die Verabschiedung der TRGS 612 „Ersatzstoffe, Ersatzverfahren und Verwendungsbeschränkungen für dichlormethanhaltige Abbeizmittel“.
Aussagen des Beschlusses 455/2009/EG
Die Neuregelung als EU-Recht, welche in allen europäischen Staaten Anwendung findet, sieht folgende Restriktionen vor:
- Betroffen sind Abbeizer, welche Dichlormethan in einer Menge größer/gleich 0,1 Gewichtsprozent beinhalten.
- Verbot des erstmaligen Inverkehrbringens an Privatpersonen oder Gewerbe nach dem 6. Dezember 2010.
- Verbot der Abgabe an Privatpersonen oder Gewerbe nach dem 6. Dezember 2011.
- Verbot der Verwendung durch das Gewerbe ab dem 6. Juni 2012.
Hiervon ausgenommen sind Gewerbe, welche durch eine Sondergenehmigung weiterhin dichlormethanhaltige Abbeizer einsetzen dürfen. Hierfür sieht der Beschluss vor, dass die einzelnen Mitgliedsstaaten Sonderregelungen treffen dürfen.
Ferner müssen seit dem 6. Dezember 2012 alle dichlormethanhaltigen Abbeizer explizit für die rein industrielle Verwendung gekennzeichnet sein.
Gründe für diesen Beschluss
Mit dem Beschluss zum Verbot dichlormethanhaltiger Abbeizer durch die Europäische Union ist ein großer Schritt in Richtung zu mehr Arbeitssicherheit gemacht worden. Die Gründe hierfür sind vielfältiger Natur:
- Es gibt keinen wirksamen Atemschutz, der vor der Inhalation von Dichlormethan schützen kann. Ein wirksamer Atemschutz kann nur durch umgebungsluftunabhängige Atemschutzgeräte bereitgestellt werden, welche im privaten Bereich überhaupt nicht, im Gewerbe nur in seltenen Fällen anzutreffen sind.
- Durch den niedrigen Siedepunkt dieser Substanz werden im Bereich des Arbeitsplatzes extrem hohe Konzentrationen dieser Chemikalie freigesetzt. Bei Messungen wurde bei schlechten Bedingungen im Freien eine fünffache, in Räumen sogar eine zehnfache Überschreitung der gesetzlichen Grenzwerte festgestellt.
- Dichlormethan steht unter Verdacht, erbgutschädigend sowie krebsauslösend zu sein.
- Seit Beginn des Einsatzes dichlormethanhaltiger Abbeizer kamen nach Angaben der Berufsgenossenschaft der Bauwirtschaft (BG BAU) in Europa 30 Menschen ums Leben. Dies rührt vor allem daher, dass Dichlormethan im Körper zu Kohlenmonoxid abgebaut wird. Bei schlechter Belüftung droht daher der Erstickungstod.
Kritik an der neuen Gesetzgebung
Bei der Verwendung von Dichlormethan-freien Abbeizern muss der Arbeitsablauf angepasst werden, da diese langsamer wirken. Sie sind aber problematisch auf 2K-Lacken und teilweise auf Kunstharzlacken. Bei den Alternativen muss auf die Art des Lackes geachtet werden, da diese nicht universell wirksam sind. Außerdem enthalten diese zum Teil andere bedenkliche Lösungsmittel wie N-Methyl-2-pyrrolidon.
Verwendung für die Entkoffeinierung
Oft wird aus Kostengründen Dichlormethan als Extraktionsmittel bei Kaffee verwendet. Dies ist laut geltendem Gesetz in Deutschland erlaubt, jedoch dürfen die Rückstände nach der Technische Hilfsstoffe-Verordnung (THV) nicht mehr als 2 mg/kg Kaffee betragen. Die zulässige Grenze im Trinkwasser und bei der Verwendung in Aromastoffen in Lebensmitteln beträgt laut THV 0,2 mg/kg.
Umweltschutz
Dichlormethan ist ein CKW und daher in vielen EU-Mitgliedstaaten für bestimmte Anwendungen komplett verboten und in Deutschland stark eingeschränkt (etwa bei der Verwendung in Textilwaschmitteln und in Reinigungsmitteln). Dies wird unter anderem in der Reach-Verordnung von 2010 geregelt. Umweltaspekte von Dichlormethan und CKWs werden in der Verordnung über genehmigungsbedürftige Anlagen (4. BImSchV) geregelt.
Ozonschicht
Mit dem Montreal-Protokoll vom September 1987 wurden die Ozonschicht zerstörende FCKW eingeschränkt. 2014 wurde erkannt, dass das Ozonloch über der Antarktis seit über 10 Jahren nicht mehr größer geworden ist. 2017 zeigen Ryan Hossaini et al. in Nature auf, dass die bisher bis 2050 erwartete Erholung der Ozonschicht – bis auf den Stand von 1980 – doch bis 2080 dauern könnte. Dichlormethan ist zwar kurzlebig und damit weniger stark ozonschädigend, da es aber in seiner (bodennahen) Konzentration von 2004 bis 2014 auf etwa das Doppelte zugenommen hat, wird dies als ursächlich für die langsame Erholung der Ozonschicht angenommen.
Risikobewertung
Dichlormethan wurde 2016 von der EU gemäß der Verordnung (EG) Nr. 1907/2006 (REACH) im Rahmen der Stoffbewertung in den fortlaufenden Aktionsplan der Gemeinschaft (CoRAP) aufgenommen. Hierbei werden die Auswirkungen des Stoffs auf die menschliche Gesundheit bzw. die Umwelt neu bewertet und ggf. Folgemaßnahmen eingeleitet. Ursächlich für die Aufnahme von Dichlormethan waren die Besorgnisse bezüglich hoher (aggregierter) Tonnage sowie der vermuteten Gefahren durch krebserregende Eigenschaften, der möglichen Gefahren durch mutagene, reproduktionstoxische und sensibilisierende Eigenschaften sowie als potentieller endokriner Disruptor. Die Neubewertung fand ab 2016 statt und wurde von Italien durchgeführt. Anschließend wurde ein Abschlussbericht veröffentlicht.
Literatur
- M. Rossberg, W. Lendle, G. Pfleiderer, A. Tögel, T. R. Torkelson, K. K. Beutel: Chloromethanes. In: Ullmanns Enzyklopädie der Technischen Chemie. Wiley-VCH Verlag, Weinheim 2012, doi:10.1002/14356007.a06_233.pub3.
Weblinks
- Dichloromethane Fact Sheet im australischen National Pollutant Inventory






